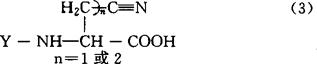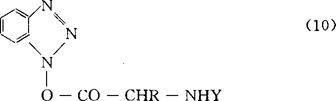| 释义 |
【固相肽合成中的接肽方法】
拼译:coupling methods in solid-phase peptide synthesis
固相肽合成法(solid-phase peptide synthesis,SPPS)自1963年由梅里菲尔德(R*B*Merrifield)首次提出其设计思路至今,经过30余年多肽化学工作者的改进和完善已成为一种十分重要和常用的多肽合成技术。其发展和推广除了归功于种类繁多的固相载体、肽链在载体上的连接和解脱方法、以及各种新型、优异的α-氨基与侧链保护基的出现外,还应归功于各种接肽方法的日趋势成熟和不断创新。在SPPS中得到普遍应用的接肽方法主要有4种:(1)直接缩合法(In situ法);(2)对称酸酐法;(3)缩合试剂/添加剂法;(4)活泼酯法。 直接将N,N′-二环已基碳二亚胺(DCC)和 保护的氨基酸的二氯甲烷溶液(有时需加部分DMF助溶)加入树脂中搅拌反应是SPPS中最早的方法(in situ DCC法)。所经过的活化中间体为高反应活性的O-酰基异脲Ⅰ和对称酸酐2。 保护的氨基酸的二氯甲烷溶液(有时需加部分DMF助溶)加入树脂中搅拌反应是SPPS中最早的方法(in situ DCC法)。所经过的活化中间体为高反应活性的O-酰基异脲Ⅰ和对称酸酐2。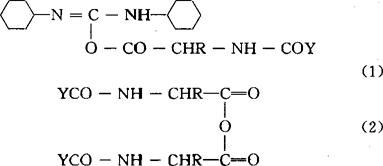
In situ DCC法操作简便,反应速度快,产率高,因而至今一直得到广泛的应用。但主要缺点是:(1)在反应中生成的副产物二环已基脲在接肽溶剂二氯甲烷中的溶解度很小,要将其洗涤除去需要花费大量的溶剂和时间,甚至虽经多次洗涤,仍会有少量吸附在树脂内部的空隙中而影响后反应。因此发展了生成的脲能溶于二氯甲烷的碳二亚胺型缩合试剂,如萨拉坦可斯(D.Sarantaksi)等1976年发现的二异丙基碳二亚胺;伊泽德白斯克(J.IZdebski)等1984年和1989年发现的特丁基乙基碳二亚胺和特丁基乙基碳二亚胺。(2)活化和缩合在一起进行,消旋副反应的产物不能预先除去,就存在连接到肽链上的危险。(3)当羧基组分为Nα-保护的Asn和Nα-保护的Gln时,不能用此法接肽,因为二者在用DCC活化时,可以发生脱水副反应生成腈化的3,3可以再次被DCC活化而连接到肽链上。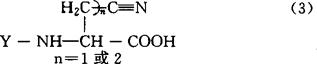
鉴于上述缺点,人们又研究发展了其他类型的缩合试剂,其中在In situ法中得到应用的有Bop(4)、PyBop(5)、HBTU(6)和Bop-Cl(7)。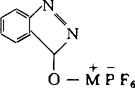
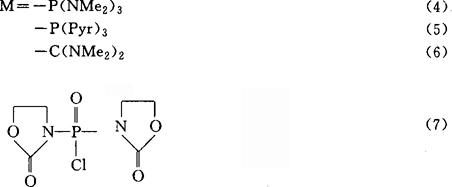
1988年阿恰纳(H.Echner)采用In situ Bop法合成了含28个残基的胸腺素α1,认为该法尤其适合连续流程的固相合成技术。连接Nα-保护Glu和His(Tos)时,和DCC法相比消旋产物比例降低。而且连接Nα-保护的Ser、Thr、Tyr时,这些氨基酸的侧链羟基可不加保护。Bop法的缺点是其反应副产物为致癌化合物HMPA,同时也不适用于Nα-保护Asn和Gln的接肽。用PyBop代替Bop则生成的副产物毒性大大降低。HBTU法比Bop法更为有效,接肽时氨基酸的侧链羟基也无需保护,而且适用于Gln和Asn的接肽。其反应副产物无毒且溶于水和二氯甲烷,易于除去。Bop-CE特别适用于立体位阻大的Nα-保护氨基酸的接肽,但其缺点是有消旋副反应。添加HOBt或咪唑可以降低产物的消旋程度。鉴于In situ DCC法实际上主要经过对称酸酐2进行的事实,1971年威拉德(T.Wieland)等提出了对称酸酐法。最常用的实验步骤是将Nα-保护的氮基酸和DCC按2∶1的比例在二氯甲烷中0℃反应15~20min,滤出析出的二环已基脲,所得对称酸酐立即用于接肽反应。Bop和HBTU也可用来制备对称酸酐。对称酸酐法的特点为:(1)反应活性高,反应速度快;(2)缩合产率高(99.6%~99.8%);(3)克服了In situ DCC法的某些缺点,如DCC与肽链的某些副反应,副产物二环已基脲难除去等。其主要缺点是原料浪费,而且同样不适于Nα-保护的Asn和Gln的接肽。对Nα,Nω-双保护的Arg也不适用,因其高活性的对称酸酐存在下式所示的副反应,生成δ-内酰胺8。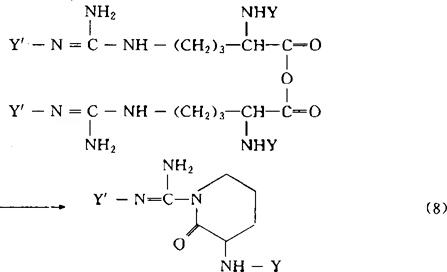
对称酸酐法的另外两个副反应为在三级胺存在下的消旋反应和下式所示的重排形成二肽9的副反应。9能被进一步活化导致微量的(≤0.3%)“夹心肽”的形成。对Gly此副反应最为严重。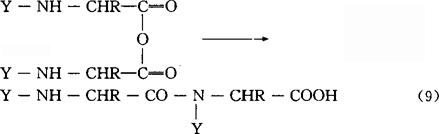
在用对称酸酐法接肽时,卡尔斯根(R.Kirstgen)、劳尔森(R.H.Laursen)、王(S.S.Wang)等报道一旦反应开始或接近完全,在反应液中添加某些碱性物质如二异丙基乙基胺、N-甲基吗啉和4-二甲氨基吡啶等可以促进反应速度。但4-二甲基氨基吡啶较少使用,因其同时也能促进消旋副反应和成二肽副反应的发生。反应液中存在DMF或添加三氟乙醇也有利于增加反应速度。1966年威敢德(F.Weygand)等人发现用DCC作缩合试剂时添加某些辅助性的亲核试剂如N-羟基丁二酰亚胺(HOSu)可以抑制DCC法中的消旋副反应和O→N迁移副反应。这一方法在SPPS中立即得到了应用。但对HOSu而言,由于它在SPPS中反应速度不理想,产率也不好,且存在下式所示的副反应,导致肽链的终止,故而在SPPS中较少用于逐步合成,较多用于片段合成。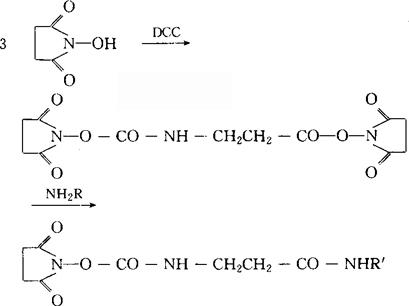
1970年凯耐格(R.Geiger)等人报道的1-羟基苯骈三唑(HOBt)是一个较好的添加剂,它不与DCC反应,因而没有象HOSu那样的副反应,而且反应速度快(接近In situ DCC法及对称酸酐法),产率高,产物的消旋程度小,还避免了In situ法中的O→N迁移副反应,因而已发展成为一种常用的固相成肽方法——DCC/HOBt法。其活化中间体主要为Nα-保护氨基酸形成的HOBt活泼酯10。该法可按两种方式操作:(1)In situ和(2)预先活化HOBt法。也可采用其它缩合试剂如Bop和Bop CE等来形成HOBt活泼酯。据汉得森(D.Hudson)报道,Bop/HOBt法反应速度大于In situ DCC法,而DCC/HOBt法则略小于In situDCC法。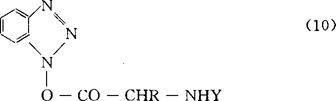
缩合试剂/HOBt法可采用于Nα-保护Asn和Gln的接肽,因为在该种反应条件下,这两种氨基酸的脱水副反应可得到抑制。但却不适于α氨基用邻硝基苯硫基、联苯异丙氧羰基(Bpoc)的氨基酸及咪唑基用于对甲苯磺酰保护的His的接肽,因为HOBt的酸性能引起这些对酸敏感的保护基的提前脱除。活泼酯法是一种久为人知并得到稳定发展的成肽方法。活泼酯一般采用在DCC或其他缩合试剂存在下将Nα-保护氨基酸和相应的羟基化合物缩合制备。活泼酯法的优点是把活化中间体变成具有一定的稳定性,可以分离,纯化和贮存但仍有相当反应活性的酯类中间体,因此一系列Nα-保护氨基酸的活泼酯曾用于SPPS中。但是,因为活泼酯的立体效应大和反应活性低等不利因素在固相合成中显得更加突出,因而成肽反应慢,产率低,而且有些活泼酯在SPPS所用的溶剂二氯甲烷中的溶解度差,这就限制了活泼酯法在SPPS中的应用。为了提高活泼酯的反应活性,人们从两个方面着手努力:在活泼酯的离去部分引入强拉电性的原子或基团来提高离去部分的离去能力和活泼酯的亲电能力;在用活泼酯接肽时添加某些添加剂如HOBt或二异丙基乙基胺来加速反应。已出现的30多种活泼酯中,在SPPS中引起人们重视的主要有邻硝基苯酯(ONo)、对硝基苯酯(ONp)、2,4,5-三氯苯酯(OTcp)、N-羟基丁二酰亚胺酯(HOSu)、五氟苯酯(Pfp)、1-羟基苯骈三唑(HOBt)、3-羟基-3,4-二氢化-4-氧化-1,2,3-苯骈三嗪(ODhbt)、2,5-二苯基-2,3-二氢化-1,B-三氧代-4-羟基噻吩酯(OTDO)、3-苯基-1-(对硝基苯基)-2-吡唑啉-5-酮(Pnp)和3-甲基-1-对硝基苯基-2-吡唑啉-5-酮(Npp)等。用ONo和ONp活泼酯接肽,反应速度慢,但可避免Asn和Gln的脱水副反应。用OTcp或Pfp酯接肽,反应速度较慢,但添加HOBt后反应速度大大加快,可接近对称酸酐法。HOSu活泼酯曾成功地用于短杆菌肽的合成,但因其前述封闭肽链的副反应,不宜推广使用。1970年凯耐格(R.Geiger)等提出的ODhbt酯是一种很有前途的活泼酯,据报道它具有和HOBt活泼酯相类似的低消旋程度和反应性质,反应速度却快于Pfp酯、接近对称酸酐法,且本身又较稳定,便于分离、纯化和贮存。OTDO酯的最大优点是产物的消旋程度极低,且其本身也很稳定,易于贮存。最近汉得森(D.Hudson)报道了Pnp和Npp酯的高反应活性,接肽反应速度居各种活泼酯之首。汉得森的实验结果表明上述各种活泼酯的反应活性顺序为:Pnp~Npp>ODhbt~DICl/HOBt>Pfp~OTDO>OTcp>HOSu>ONp>ONo。此外,在用ODhbt、OTDO、Pnp和Npp接肽时,可通过反应完成前后颜色的变化监测反应进行的完全程度。除了上述肽链形成的方法外,液相合成中大多数其他成肽方法如迭氮化物法、混合酸酐法、四组分缩合法等都曾在SPPS中应用过,但由于各自的缺点而没有得到推广。尽管如此,其它方法在某些特定条件下的作用也不能忽视。值得指出70年代中期由麦特休德(R.Matsueda)等人提出的氧化还原缩合法和近年来中外学者提出的活泼酰胺法在SPPS中仍有很大的潜力。如上所述,各种接肽方法各有其优点和局限,在实际工作中人们往往把不同的方法结合起来,取长补短,以满足肽合成的复杂需要。同时,进一步发展和完善现有成肽方法、探索新型缩合试剂仍然是发展固相肽合成技术的一个重要而艰巨的任务。【参考文献】:1 Merrifield R B. J Amer ChemSoc, 1963 ,85 :2149~21542 Wolters E T M, et al. J Org Chem, 1974,39:3388~33923 Yamashiro D, et al. J Amer Chem Soc, 1978,100:5174~ 51794 Birr C. Aspects of the merrifield peptide synthesis.Springer-Verlag,Berlin Heidelberg, New York,19785 Merrifieldll R B. Angew Chem, 1985,97:801~8126 黄惟德,等.多肽合成.北京:科学出版社,1985,202~2057 Barany G, et al. Int J Peptide Protein Res, 1987,30:705~ 7398 Field G B, et al. Int J Peptide Protein Res 1990,35:161~ 2149 Hudson D. Chemistry, structure and Biology Leiden:ESCOM,1990,914~91510 田少雷,等.化学通报,1992,2∶17~22(中国医药研究开发中心田少雷副研究员撰;蔡孟深审) |
 保护的氨基酸的二氯甲烷溶液(有时需加部分DMF助溶)加入树脂中搅拌反应是SPPS中最早的方法(in situ DCC法)。所经过的活化中间体为高反应活性的O-酰基异脲Ⅰ和对称酸酐2。
保护的氨基酸的二氯甲烷溶液(有时需加部分DMF助溶)加入树脂中搅拌反应是SPPS中最早的方法(in situ DCC法)。所经过的活化中间体为高反应活性的O-酰基异脲Ⅰ和对称酸酐2。